Данный пост о валидации процессов очистки состоит из следующих разделов
- Вводные данные о производств
- Подготовка необходимых данных (таблиц)
- Определение допустимого уровня загрязнения по методу “наихудшего случая”.
- Аналитические методики
- Процедура очистки
- Отбор проб
- Анализ
Результаты
1. Вводные данные о производстве
Все что описано далее обусловлено этим и только этим.
производство дженериков 20 наименований ЛС + балк, класс чистоты Д, Оборудование пара грануляторов, V-миксер, 2 таблетпресса и капсулятор, дражировальный котел, пара блистерных линии и банка. В общем типовой заводик коих на территории постсоветского пространства понастроено (модернизировано) немало.
Идея наихудшего случая предполагает что у вас на одном том же оборудовании производятся разные препараты и так как проводить валидацию очистки от каждого препарата дорого сложно физически невозможно и экономически нецелесообразно 🙂 (почему узнаете ниже), то валидация очистк проводится на одном самом вредном препарате. Надо отметить что главное не то что оборудование одинаковое, а то что отмывается одинаково, т. е. процессы очистки одни и те же.
2. Подготовка необходимых данных (таблиц)
2.1. Составить перечень оборудования подлежащего валидации очистки с указанием площадей контакта с продуктом и подлежащей очистке, с указанием СОП по очистке и вида очистки.
****
Самый трудный момент это определение площадей оборудования контактирующего с продуктом. Если оборудование новое от 2007 года примерно, все площади указаны в документации, если все оборудование старое, находим в инете как считать площади фигуг, берем рулетку блокнот и калькулятор и идем считать.
****
На выходе получим вот такую таблицу.
| № | Оборудование | Модель | Площадь | Вид очистки | СОП по очистке | Код (ГФ) |
2.2. Составить перечень выпускаемых препаратов с указанием размера загрузок, терапевтической и максимальной дневной дозы. Составить таблицу загрузок для разного оборудования.
****
Для этого надо узнать план продаж на следующий год. Нет, можно конечно посмотреть в приложениях к лицензии, но тогда список увеличится в разы. Затем открываем досье на препарат и берем данные оттуда, LDD в инструкции по применению. Составить таблицу загрузок для разного оборудования. – имеется ввиду что если масса сначала мешается в пьяной бочке, затем идет в роторный гранулятор, затем в гранулятор псевдокипящего слоя, затем в тритурационную колонну (ессно только на бумаге) то для каждого вида оборудования пишем размер загрузки.
****
| № | Наименование | Загрузка | TD | LDD |
| 1 | Герпевир | 102,8 | 25 | 400 |
2.3. Составить перечень выпускаемых препаратов и связанного с ним технологического оборудования.
Т.е. составляем таблицу
| № | Наименование препаратов | Оборудование |
| 1 | Герпевир | ГФ-43, ГФ-45, ГФ-74, ГФ-61 |
2.4. Составить перечень выпускаемых препаратов с указанием растворимости используемых субстанций.
2.5. Составить перечень используемых детергентов.
На этом этапе вы имеете все необходимые таблицы. Тут надо все таблицы проверить что бы ошибка не тянулась дальше и вспомнить про мертвых душ. Это оборудование которое есть в СОПах и регламентах, но которое вы забыли. Например, вибросито, детектор металлов, просмотровая машина, большой миксер, где якобы происходит объединение серии и т.д.
3. Определение допустимого уровня загрязнения по методу “наихудшего случая”.
Произвести расчет МАС – максимально допустимого количества остатков на поверхности оборудования для всех выпускаемых на нем препаратов. По формуле: 0,1% обычной терапевтической дозы одного продукта, который может быть в дневной дозе последующего продукта.
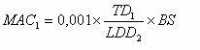 ТD – индивидуальная терапевтическая доза подконтрольного продукта;
ТD – индивидуальная терапевтическая доза подконтрольного продукта;
ВS – размер серии последующего продукта. В последующих расчетах используется масса одной стандартной загрузки в V-образном смесителе;
LDD – максимальная дневная доза последующего продукта.
Я расчет провожу в программе Excel. Для этого строю таблицу.
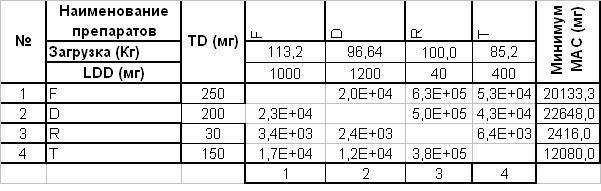 Поясню, по вертикали и по горизонтали одни и те же препараты. По горизонтали препарат который выпускается первым и после которого происходит отмывка. По вертикали следующий препарат. Самое маленькое число в матрице это и есть наихудший случай.
Поясню, по вертикали и по горизонтали одни и те же препараты. По горизонтали препарат который выпускается первым и после которого происходит отмывка. По вертикали следующий препарат. Самое маленькое число в матрице это и есть наихудший случай.
Такая таблица строиться для каждой единицы оборудования на которой производится несколько единиц продукции. Да-да для каждой. Ну кроме тех где продукты одинаковые. У вас получится 5 – 10 таких таблиц. Но нас интересуют самые маленькие значения а они там, где много препаратов, маленькие дозировки и маленькие загрузки.
Дальше – выбор наихудшего случая.
Из каждой таблицы выбираем три наихудших случая, (я так решил) минимальных значения, и смотрим на каком оборудовании возможна перекрестная контаминация. Определяем это оборудование и определяем площадь возможной контаминации. Не забываем про тару пластиковую и из нержавейки. Она вносит очень существенный вклад.
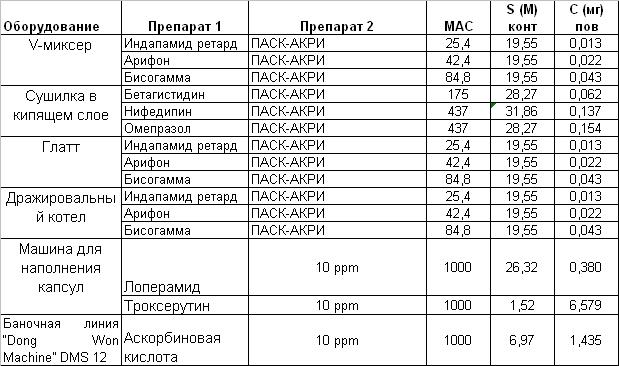
Смеситель – оборудование на котором задействовано самое большое количество выпускаемых препаратов. Препарат 1 – тот от которого происходит отмывка имеет самую маленькую TD, Препарат 2 – имеет самую большую LDD. MAC- величина рассчитанная по формуле, S(M) площадь перекрестной контаминации. С мг пов – концентрация на площади пробоотбора, т.е сколько его будет в пробе. Из этой таблицы видно что наихудший случай это препарат индапамид ретард выпускаемые перед препаратом ПАСК-АКРИ. перекрестная контаминация возможна на миксере, Глатте,таблетпрессе, дражировальном котле и блистерной машине. Не забываем про тару. Складываем все полученные площади и вносим ее в ячейку S(M). МАС берем из предыдущей таблицы. С мг пов равен МАС делить на площадь и умножить на площадь пробоотбора, с поправко на разбавление если надо. Валидация очистки тары, пробоотборников, и другого вспомогательного оборудования проводится на индапамиде ретарде. Для валидации очистки другого оборудования выбирается другие препараты. Если в банку ничего кроме аскорбинки не фасуется, то берем аскорбинку как критический препарат. критерий 10 ppm.
Детергенты
Для каждого детергента подсчитать максимальное количество остатков на соприкасающихся поверхностях.
Формулы расчета:
МАС = ADI х BS / LDD
ADI = NOEL х AAW х SF
NOEL = LD50 х EF
При подсчете допустимого остаточного количества моющего средства для определения «наихудшего» случая, предполагается, что вся технологическая линия может быть очищена одним из заявленных детергентов.
Формула расчета: DLPМС = МАСМС х A/F
MAC – Maximum allowable carryover, максимально допустимое количество вещества, которое может оставаться на поверхности оборудования после очистки;
ADI – acceptable daily intake, приемлемый суточный прием;
BS / LDD – количество суточных доз последующего продукта;
NOEL – no observated effect level, уровень отсутствия эффекта;
AAW – average adult weight, средний вес взрослого человека (70 кг)
TD – Theurapeutical dose, терапевтическая доза;
SF – Safety factor, фактор безопасности (коэффициент безопасности), для пероральных препаратов, как правило, принимается равным 1/1000 (т.е. SF=0,001);
LD50 – средняя смертельная доза
EF – empirical factor, эмпирический фактор Лейтона, отражающий перенос модели с крыс на человека (равен 0,0005);
| № | Наименование | Класс опасности | LD50 (мг/кг) |
| 1 | Тефлекс | 4 | >5000 |
| 2 | Новодез-форте | 4 | >5000 |
| 3 | Дезин (водный) | 4 | >5000 |
| 4 | Аламинол плюс | 4 | >5000 |
| 5 | Жавель-солид | 3 | 151-5000 |
| 6 | Ника-экстра М | 4 | >5000 |
| 7 | Макси- дез | 4 | >5000 |
| 8 | Ника-Неодез | 3 | 151-5000 |
Собссна вся недолга. Теперь сами анализы и проблема аналитических методик.
4. Аналитические методики
Теперь мы знаем сколько и какого вещества должно быть в пробе и можно приступить к разработке метода анализа.
****
Тут надо отметить следующее. Я не знаю как это делается и буду очень рад если кто либо напишет про это и особенно про ресурсоемкость этих мероприятий. В лавке где я работаю исторически сложилось следующее. После каждой очистки оборудования берутся смывы на СФ. Для валидации ставят ТСХ. Сейчас провели расчеты и вроде чувствительности хватает для СФ. Но вопрос селективности остается очень открытым.
****
5. Процедура очистки
Если коротко, то как получится так и отмоем и вообще, если говорить серьезно, то стандартизовать этот процесс не представляется возможном. Сейчас немцы предлагают оборудование, которое в автоматическом режиме отмывает оборудование (гранулятор) так что он пойдет валидацию. Давление воды 16 бар. Это конечно гут, но как быть с таблетпрессом? Для того что б снять все эти вопросы о валидации процессов очистки начинаем говорить только тогда, когда оборудование визуально чистое. Мое мнение.
СОП по очиске каждой единицы оборудования имеется. Без вопросов.
6. Отбор проб
В ОКК есть соп по отбору проб, где указаны все точки отбора. Люди которые на этом оборудовании работают прекрасно их знают и помощь ООК здесь не требуется. Кстати на каждую единицу от 5 до 15 точек. Для производства Индапамид ретард используется около 10 единиц крупного оборудования + тара и пробоотборники. Количество ТСХушек посчитали? Вот. СФ быстрее.
7. Анализ
Анализ делают сменные химики ОКК по сопу и ранее утвержденной методике, проблем тут нет, обычно все хорошо. Детергент определяется качественной реакцией с реактивом Несслера. Необходимо добавить, что очистка оборудования проводится после выпуска группы серий, тоесть при переходе с одного препарата на другой. Это значит что три процесса очистки могут растянуться на год и более.
Результаты
Что получится узнаешь когда взрослые придут (с).
PS to Optisemist.
Буду очень рад если вы напишете тему по расчету МАС на буржуйском форуме.
Вопросы те же что и у меня.
- Считаете ли вы МАС?
- Если считаете то какой он у вас получился? (цифру!) Сам МАС и содержание действующего вещества в пробе?
- Методика анализа ТСХ, СФ ВЭЖХ?
- Анализируете ли вы чистоту оборудоваия после смены препарата или достаточно показателя “Визуально чисто” и протокола валидации процесса очистки?
кто дочитал тем спасибо 😀









А у меня вот такой вопрос. Как вести разработку методик по очистке, если эти нормы подвижны. Они могут варьировать в достаточно широком диапазоне концентраций. Например, написал методику на железо (III) гидроксид сахарозный комплекс, с привязкой к норме 5 мг/л. Через пару месяцев норма сменилась на 0,75 мг/л, это почти в 7 раз ниже. Да, этой методикой можно определить такое количество, но это уже ПКО методики. Что я неправильно делаю, объясните пожалуйста.
А у меня вот такой вопрос. Как вести разработку методик по очистке, если эти нормы подвижны. Они могут варьировать в достаточно широком диапазоне концентраций. Например, написал методику на железо (III) гидроксид сахарозный комплекс, с привязкой к норме 5 мг/л. Через пару месяцев норма сменилась на 0,75 мг/л, это почти в 7 раз ниже. Да, этой методикой можно определить такое количество, но это уже ПКО методики. Что я неправильно делаю, объясните пожалуйста.
Познавательная статья, но есть еще каша в голове. С кем можно пообщаться на тему валидации? (можете оставить почту свою)?
Дарья, можете задавать вопросы на форуме и пройтись по уже озвученным темам через поиск.
Почту вряд ли кто-то оставит по причине спама. Но на форуме есть личные сообщения. Через них можно общаться.
Здравствуйте. Я только начала заниматься валидацией очистки. Подскажите пожалуйста – Определения остатков действующих и вспомогательных веществ в смывах, методом титрования – это вообще возможно? Вот мы взяли смыв с нашего оборудования, и этот смыв мы потом титруем (по валидированной методики) – мне кажется, что титрование не сможет вообще ничего показать. А другого оборудования у нас нет, только СФ. Но и для того, чтоб определять на СФ нужно разработать методику, подобрать соответствующие условия и опять же ее валидировать.
И вопрос на остатки детергента, как его определять? ?
Посоветуйте пожалуйста.
Добрый день! Столкнулись с вопросом: после произведенного продукта (одно API, нерастворимо в воде) должен производится продукт, имеющий в своем составе 5 API (из них 3 нерастворимы в воде и имеют разные дозировки). Вопрос- как считать MSC (МАС)? По какому из API или по всем трем нерастворимым? И как потом рассчитывать MSSR?
Добрый день! Спасибо за статью!
У меня следующий вопрос: я рассчитала MAC 0,684 мг, также имеется емкость, площадь контакта которой с действующим веществом 1970 см2. Метод отбора проб, используемый после очистки емкости, при помощи промывных вод. ПО методики (ИФА) 0,01 МЕ/мл или 80 пг/мл. Для анализа химикам нужен только 1 мл промывных вод.
Как рассчитать объем промывных вод, который потребуется для данной площади? Есть ли какие-то рекомендации по этому поводу?
Коллеги, добрый день!
Кто знает какие программы существую (калькуляторы) для пересчета комбинаций пар при определении “наихудшего случая” в процессе валидации очистки?
Lessie, перенес два ваших последних вопроса на форум. В комментариях к статье отвечают реже.
Коллеги, поделитесь опытом. Как вы считаете процесс повреждения оксидной пленки на поверхности нержавеющей стали 316 (царапины) мог привести к образованию белого налета в это месте, который не удаляется с помощью воды и спирта этилового 70%, 95%. Оборудование используется для загрузки порошков (АФС + вспомогательные).
Заранее благодарю вас.
Добрый день, коллеги! Спасибо большое за статью. Но меня все же мучает вопрос, как быть с растворимостью (трудность в очистке) продукта? В данной статье рассматривается вариант выбора “наихудшего случая” с учетом расчета MAC при переходе из продукта А в продукт Б. Однако, если такой переход определен, и “наихудшим” выбран продукт А, но по факту продукт С практически нерастворимый, липкий и большое кол-во серий. Как быть? Что будет являться “наихудшим случаем”? Или их будет два? Заранее очень вас благодарю.
Спасибо большое.
Добрый день! Помогите с проблемой!
В случае ручного процесса очистки , что будет являться “наихудшим случаем” если очистка прошла в 3-х циклах при одинаковых условиях, но за разное время, получены одинаково удовлетворительные результаты. Первый цикл -очистились за 5 минут, второй цикл прошел за 3 минуты, третий цикл прошел за 7 минут. Какое время считать приемлемым “наименьшее время” 3-минуты (в каждом из 3-х циклов мы одинаково хорошо очистили оборудование) или все -таки 7 минут (поскольку у нас нет 3-х результатов по 3 минуты, чтобы принять время 3 минуты)?
Заранее благодарю.
Относительно минимальных терапевтической дозы – изучите инструкцию, там эта информация должна быть.
Интересно написанная статья. Я только в начале пути, впервые пришлось заниматься валидацией. Данная статья предназначена для твёрдых лекарственных форм (ТЛФ), а, а что делать если у нас мягкие лекарственные формы и как делать расчет mac, как узнать минимальную терапевтическую дозу, если она не прописывается и где узнать SFi для мягких лекарственных форм?
Спасибо за статью. Очень полезно.
Только есть такой момент. При таком подходе при определении worst case не учитывается растворимость и сложность удаления АФИ.
Добрый день, уважаемый Kirillcheg!
Помогите пожалуйста: при расчете МАС по формуле
MAC1 = 0,001 x TD1 / LDD2 x BS
возникли вопросы:
1. TD (индивидуальная терапевтическая доза подконтрольного продукта) – правильно ли я понимаю, что это минимальная суточная доза умноженная на минимальный курс лечения?
Например: Препарат применяют внутрь, после еды. Лечение начинают с дозы 20 мг, распределенной на два приема по 10 мг в течение дня (утром и днем). При недостаточной эффективности терапии и при хорошей переносимости препарата дозу повышают до 30 мг, распределяя ее на три приема по 10 мг в течение дня. Не следует принимать препарат позднее 18 часов. Длительность курсового лечения составляет 1,5 – 3 месяца. Повторный курс лечения при необходимости может быть проведен через 1 месяц.
TD = 20 мг х 45 дней = 900 мг
2. Как вычислить TD, если в инструкции МП написано:
Лечение начинают с дозы 300 мг внутрь один раз в сутки и постепенно увеличивают до 900 мг/сут (первый день – 300 мг один раз в сутки, второй – по 300 мг два раза в сутки, третий – по 300 мг три раза в сутки). В последующем доза может быть увеличена. Обычная доза препарата составляет 900-1200 мг в сутки. Максимальная доза – 3600 мг/сут, разделенная на три равных приема через 8 часов.
Статьи познавательные. Автору и сайту – большая благодарность.
Сам только приступаю заниматься валидацией на аналогичном предприятии в Восточной Сибири.
И подход мой к очистке схож: да, надо посчитать дозы, но надо бы еще применить метод модельных смесей. Иными словами не следует валидировать подход производства (моем, пока не станет чисто), а более-менее около научный подход: знаем сколько вещества нанесли на поверхность (имеется в виду, что выбрали “наихудший” случай не по растворимости активного вещества, а по отмывке этого вещества в смеси со вспомогательными (согласно используемой прописи)), проводим очистку по стадиям согласно СОП по очистке (сухая, влажная 1 проход, влажная 2 проход и т.д.). После каждого прохода берем пробы и смотрим сколько вещества сняли с поверхности и сколько осталось. И так до того, пока не обнаружим, что степень очистки соответствует критерию приемлемости.
Этот подход даст много информации для производства. Необходимый минимум промывов из рекомендаций протокола валидации плавно перетекает в СОП по очистке. И время на отмывку становится известным и научно доказанным.
Возможно это всем очевидно, тогда извиняюсь за словоблудие.
Сам, кстати, открыл для себя и для производства многоведерную систему для очистки (см. Уайта).
На мой взгляд наиболее эффективный подход к валидации очистки:
1. Рибофлавиновый тест (предвилидация совмещенная с обучением операторов и демонстрации им “критических” зон). К сожалению не всегда применим.
2. Валидация очистки с применением отвалидированного метода взятия и анализа смывов (желательно ВЭЖХ). При этом использовать информацию по критическим зонам определенным по результатам рибофлавинового теста. Саму технику вы описали: расчет МАС, определение площади переноса и т.д…
3. “Отлов” нерадивых операторов методом контроля общего органического углерода (ООУ) в смывах периодически или постоянно.
Анализ смывов на ООУ требует особой техники взятия смывов. Метод эффективен для взятия смывов с мест труднодоступных для визуальной оценки. Метод не идеальный, но во всяком случае лучше чем pH и кондуктометрия, т.к. мене специфичен к очищаемым компонентам.
Применение СФ и ТСХ для рутинного контроля чистоты надо оценивать индивидуально. Могу сказать, что пока не встречал ни одного достаточно специфичного метода СФ. Как правило вещество в смыве разбавлено настолько, что его поглощение света практически не отличается от суммарного поглощения раствора. Для более точного определения активный компонент необходимо концентрировать методом хроматографии. ВЭЖХ – предпочтительнее, так как более избирательный. ТСХ, на мой взгляд, очень субъективный метод в принципе, для валидации я бы его не применял. Для рутинного контроля ТСХ применять можно, предварительно подтвердив его эффективность методом ВЭЖХ.
Не он один дочитал до конца 😀 Просматриваю буржуйский форум, который generationP рекомендовал (askaboutvalidation.com), чтобы не дублировать. Форум, кстати, изрядный. У них не то, что отдельная тема про валидацию очистки, а целый раздел – больше 300 тем. Не то, чтобы каждая содержала информацию, но кой-чего есть. Полезное переведу в исходную тему, на выходных наверное 🙄
Весьма позновательно! Дочитал до конца 🙂