В заголовок вроде бы как вынесена крамола. Но при ближайшем рассмотрении выяснится (и очень быстро при этом), что не совсем. Многочисленные семинары говорят нам «по инерции» (вызванной традиционным квалификационным подходом), мол, на стадии IQ мы проверим монтаж, на стадии OQ мы прощёлкаем такие-то кнопки/функции и т.п. Причем семинары достаточно высокопоставленные! ECA в солнечной Германии, британские CVS, FAVEA, в Руководстве ГИЛС и НП «Целостность данных и валидация компьютеризированных систем» также предложено разбиение на эти фазы. Но есть пару «но» ?
Валідація компʼютеризованих систем
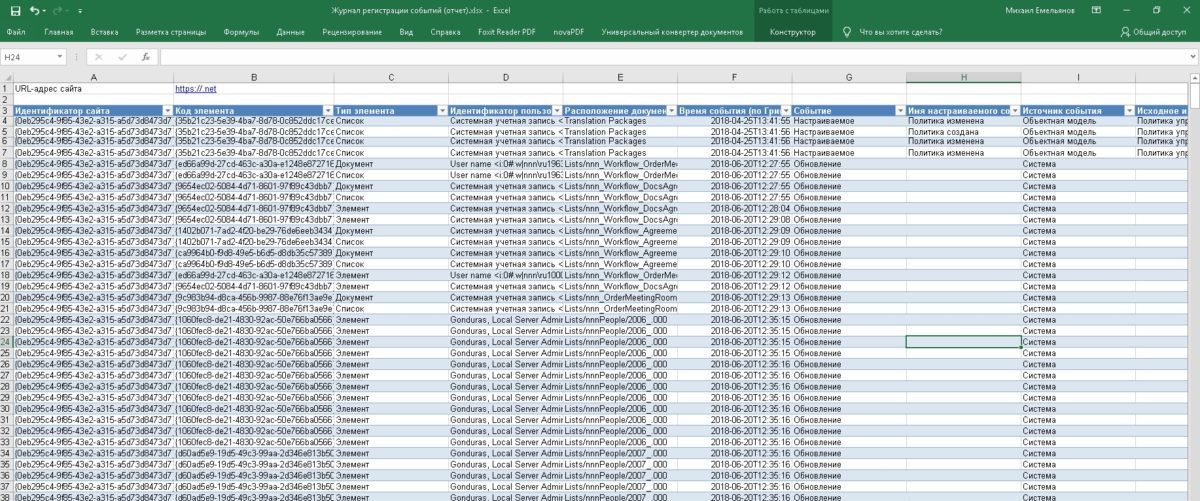
Заметки на просторах. Валидация КС
Аккумуляция опыта по валидации компьютеризированных систем дает возможность представить некоторые интересные случаи. Авторы не бьют себя пяткой в грудь, но продвигаются в данном вопросе постоянно вперед.
Квалификация или валидация компьютеризированных COTS-систем лаборатории
За последние два десятилетия достижения в области технологий проведения испытаний позволили в значительной степени расширить функциональные возможности и контроль лабораторных приборов с помощью специализированного программного обеспечения (ПО). В дополнение к этому, повышение внимания со стороны регуляторных органов к защищенности и безопасности данных привело к тому, что это ПО стало в большей степени соответствовать нормативным требованиям.
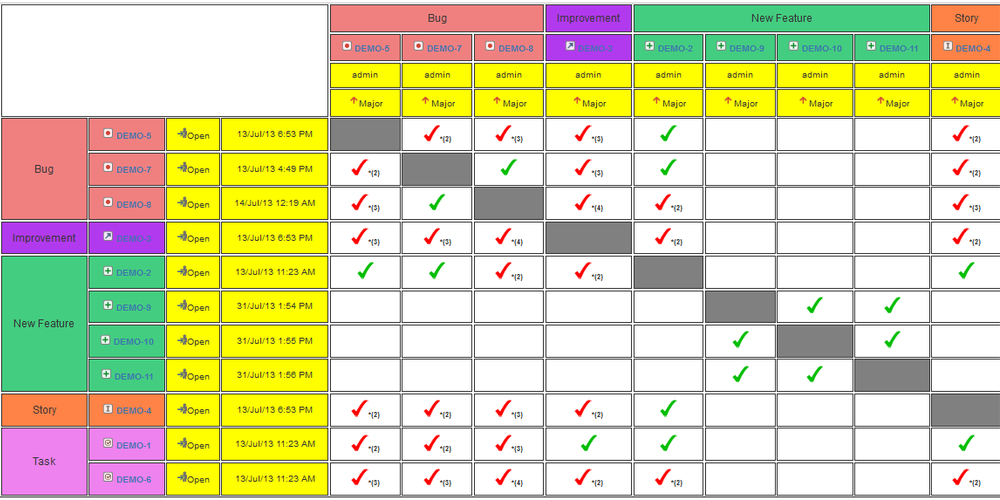
Матрица прослеживаемости для валидации процесса
Вот представьте себе ситуацию – пришлось вам как-то проводить валидацию.
Вы подготовили для этого валидационный план, выполнили все его пункты, квалифицировали все необходимое оборудование, разработали, проверили и ввели в эксплуатацию средства контроля вашего процесса. Выполнили IQ, OQ и PQ. Утвердили все чертежи и процедуры. Провели обучение и все хорошо задокументировали. Ваш итоговый отчет гордо свидетельствует о том, что все запланированные работы были выполнены успешно, а все исключения были подобающим образом разрешены.
12 способов снижения рисков для целостности данных
Это вводная статья перед более серьезной статьей на тему целостности данных, которая будет опубликована позже.
За последние года целостность данных приобрела статус серьезной проблемы и находится в центре внимания многих предприятий. FDA в свою очередь опубликовало руководство по целостности данных, в котором изложены принципы соблюдения текущих требований GMP и затрагивается роль целостности данных для промышленности.