Как известно, в руководстве FDA квалификация не выделяется в качестве обособленной процедуры, вместо этого она рассматривается как подкласс валидации и как правило проводится в рамках полномасштабных валидационных мероприятий или в их поддержку.
требование
Об идентификации
В основных процессах к причинам неправильной, несвоевременной или отсутствующей идентификации продукта относят большинство несоответствий. Очень часто эти случаи ведут к затратам на устранение брака. Именно поэтому требования к идентификации есть во всех стандартах на системы менеджмента, в требованиях клиентов, нормативных государственных и отраслевых документах.
Стандарт ISO 9000 не дает определения термина «идентификация», но в ISO 9001 требования к идентификации встречаются для двух целей:
Где это вообще написано?
Вопрос: наш отдел обеспечения качества (ООК) занимается организацией обучения сотрудников всех уровней нашей компании. В ходе занятий мы раздаем учебные материалы, в которых указываем ссылки на различные нормативные документы, применительно к конкретной теме. И вот в ходе проведения обучения мы столкнулись с сотрудниками, которые усомнились в том, что в нашей системе качества соблюдаются нормативные требования. Они утверждают, что не могут найти подобные требования в нормативных документах. Знания сотрудников ООК ставятся под сомнения, и они с трудом находят поддержку со стороны всех остальных сотрудников. Как мы можем решить данную проблему?
Квалификация или валидация компьютеризированных COTS-систем лаборатории
За последние два десятилетия достижения в области технологий проведения испытаний позволили в значительной степени расширить функциональные возможности и контроль лабораторных приборов с помощью специализированного программного обеспечения (ПО). В дополнение к этому, повышение внимания со стороны регуляторных органов к защищенности и безопасности данных привело к тому, что это ПО стало в большей степени соответствовать нормативным требованиям.
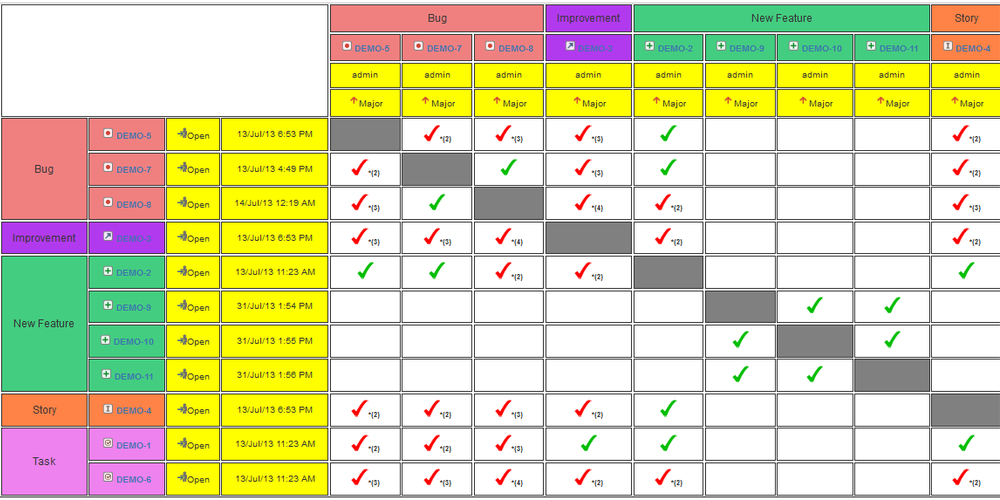
Матрица прослеживаемости для валидации процесса
Вот представьте себе ситуацию – пришлось вам как-то проводить валидацию.
Вы подготовили для этого валидационный план, выполнили все его пункты, квалифицировали все необходимое оборудование, разработали, проверили и ввели в эксплуатацию средства контроля вашего процесса. Выполнили IQ, OQ и PQ. Утвердили все чертежи и процедуры. Провели обучение и все хорошо задокументировали. Ваш итоговый отчет гордо свидетельствует о том, что все запланированные работы были выполнены успешно, а все исключения были подобающим образом разрешены.