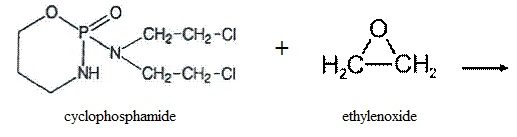shved, спасибо за интересный вопрос.
ИМХО, циклофосфамид находится у Вас в кристаллическом состоянии, а один из минусов EtO-стерилизации, то что газ плохо проникает в кристаллические структуры.
Disadvantages of ethylene oxide gas sterilisation
- Does not permeate crystals
- The levels at which it is detected exceeds safe humans for humans
- Toxicity includes burns, blistering, headache, dizziness, nausea and vomiting, weeping (lacrimation)
- Needs to be completely removed from treated products (e.g. rubber gloves) to avoid skin reactions
- Explosive mixtures are formed with air at concentrations above 3%
- Humidity may decrease activity
Стоит, наверное, еще задуматься по поводу того, что остаточные количества придется контролировать в готовом препарате при выпуске, поскольку EtO проявляет канцерогенное, мутагенное, раздражающее и наркотическое действие.
EtO вроде как чаще используется для стерилизации мед. техники (там где есть электроника), мед. изделий.
На счет реакции, я думаю хоть поверхностная но произойдет. Все таки эпоксид, а циклофосфамиду есть чем восстанавливать.
Кстати, вот еще цитата из USP, но я думаю Вы её знаете:
The choice of gas sterilization as an alternative to heat is frequently made when the material to be sterilized cannot withstand the high temperatures obtained in the steam sterilization or dry-heat sterilization processes. The most commonly employed method of gaseous sterilization is ethylene oxide. Among the disadvantages of ethylene oxide are its highly flammable nature unless mixed with suitable inert gases, its mutagenic properties, and the possibility of toxic residues in treated materials, particularly those containing chloride ions. The sterilization process is generally carried out in a pressure and vacuum-rated chamber designed similarly to a steam autoclave but with the additional features (see below) unique to sterilizers employing this gas. Facilities employing this sterilizing agent should be designed to provide adequate post sterilization degassing, to enable microbial survivor monitoring, and to minimize exposure of operators to the potentially harmful gas.2
Validation of a sterilizing process employing ethylene oxide gas is accomplished along the lines discussed earlier. However, the program is more comprehensive than for the other sterilization procedures, because in addition to temperature, the humidity, vacuum/positive pressure, and ethylene oxide concentration also require appropriate parametric control. An important determination is to demonstrate that all critical process parameters in the chamber are adequate during the entire cycle. Because the sterilization parameters applied to the articles to be sterilized are critical variables, it is frequently advisable to precondition the load to achieve the required moisture content in order to minimize the time of holding at the required temperature before placement of the load in the ethylene oxide chamber. Validation is generally conducted employing product inoculated with appropriate BIs such as spore preparations of Bacillus atrophaeus. For validation they may be used in full chamber loads of product, or simulated product. The monitoring of moisture and gas concentration requires the utilization of sophisticated instrumentation that only knowledgeable and experienced individuals can calibrate, operate, and maintain. BIs may also be employed in monitoring routine runs.
As is indicated elsewhere in this chapter, the BI may be employed in a fraction negative mode to establish the ultimate microbiological survivor probability in designing an ethylene oxide sterilization cycle using inoculated product or inoculated simulated product.
One of the principal limiting factors of the ethylene oxide sterilization process is the limited ability of the gas to diffuse to the innermost product areas that require sterilization. Package design and chamber loading patterns therefore must be determined to allow for necessary gas penetration. The reader is referred to ISO 11135 for a complete description of process development, validation, and routine control of ethylene oxide sterilization processes.
Один из побочных эффектов. Может рвануть 👿 , особые меры безопасности при проведении стерилизации.
Если б все так просто было, окисью этилена бы все стерилизовали.
Но активная она. Со вторичной аминогруппой прореагирует легко.
Всё равно буду пробовать. Надеюсь что контаминация поверхностная и внутрь кристаллов EtO проникать не понадобится. Остаточное колличество EtO проконтролируем после аерации на газовом, главное чтобы после всех процедур циклофосик целый остался. Имел уже с ним отрицательный результат после гамма-облучения. В реультате облучения дозой 25 кГр субстанция приобрела коричневый цвет (изначально - белый или почти белый кристлич порошок), а примеси даже не проверял так как уже "Описание" не проходит. Термические методы не подходят - температура плавления субстанции 49-53С, а при 60С уже начинается разложение. Начальная контаминация минимальная. Думаю попробовать облучить 5 кГр, но надежды мало так как доза ну очень низкая.
Если вы пытаетесь "спасти" забракованную по микробиологической чистоте субстанцию - не старайтесь. Ничего хорошего из этого не выйдет 🙁
Даже если у вас получится улучшить один показатель, то посыпятся другие, не говоря уже о сроке годности продукта.
Как говориться: "из г....а конфетку не сделаешь".
@shved писал(а):
Имел уже с ним отрицательный результат после гамма-облучения. В реультате облучения дозой 25 кГр субстанция приобрела коричневый цвет (изначально - белый или почти белый кристлич порошок), а примеси даже не проверял так как уже "Описание" не проходит. Термические методы не подходят - температура плавления субстанции 49-53С, а при 60С уже начинается разложение. Начальная контаминация минимальная.
Возможно стОит попробовать стерилизацию (ПБЭ) потоком быстрых электронов... Где-то читал, что время набора макс. дозы стерилизации потоком быстрых электронов составляет 20-30 сек., у гамма-излучения - 5-6 часов. В Киеве, по-моему, имеется линейный ускоритель электронов...
Думаю попробовать облучить 5 кГр, но надежды мало так как доза ну очень низкая.
Не знаю, как этот вид стерилизации (имеется в виду ПБЭ) повлияет на цвет стерилизуемого материала, но для разрушения того же вирусного гепатита В и С нужна доза 40-50 кГр.
Обдумывал и этот вариант. Но решил что смысла пробовать нет, так как стерилизующее действие излучения ПБЭ и гамма в принципе одинаковое. Происходит гидролиз молекул воды в субстанции с образованием радикалов, которые и являються стерилизующим агентом (насколько помню - негативное действие на ДНК). Так как субстанция в виде моногидрата, воды в ней хватает. Вот эти радикалы думаю и сам циклофосик разваливают.
Кому интересно - статья (Radiation effect studies on anticancer drugs, cyclophosphamide and doxorubicin for radiation sterilization) по радиационной стерилизации циклофосфамида - те же результаты.
Я сразу не заметил - цитата из USP:
the possibility of toxic residues in treated materials, particularly those containing chloride ions.
У меня же в молекуле два атома хлора. Я так понимаю это как раз про мой случай. Ещё статью прочитал о последствиях газовой стерилизации ПВХ плёнки. В моём случае эти процессы будут происходить?
Чем закончилась история? "Спасли" субстанцию? 🙂
История пока ещё не закончилась, спасаем... 😥